이온화합물1을 분리,분석하는 장비입니다.
우선 이온(ion)이라는 것부터 알아볼까요.🤓
대표적으로 양이온(+)과 음이온(-)이 존재합니다.
아래 표로 구분해 놓았습니다.
| 구분 | 내용 |
| 양이온 (Cation) | 전자를 잃어버린 원자나 분자 |
| 음이온 (Anion) | 전자를 얻은 원자나 분자 |
그럼 누가 양이온이 되고 누가 음이온이 되는 걸까요?
자 우리가 좋아하는 주기율표입니다.😀
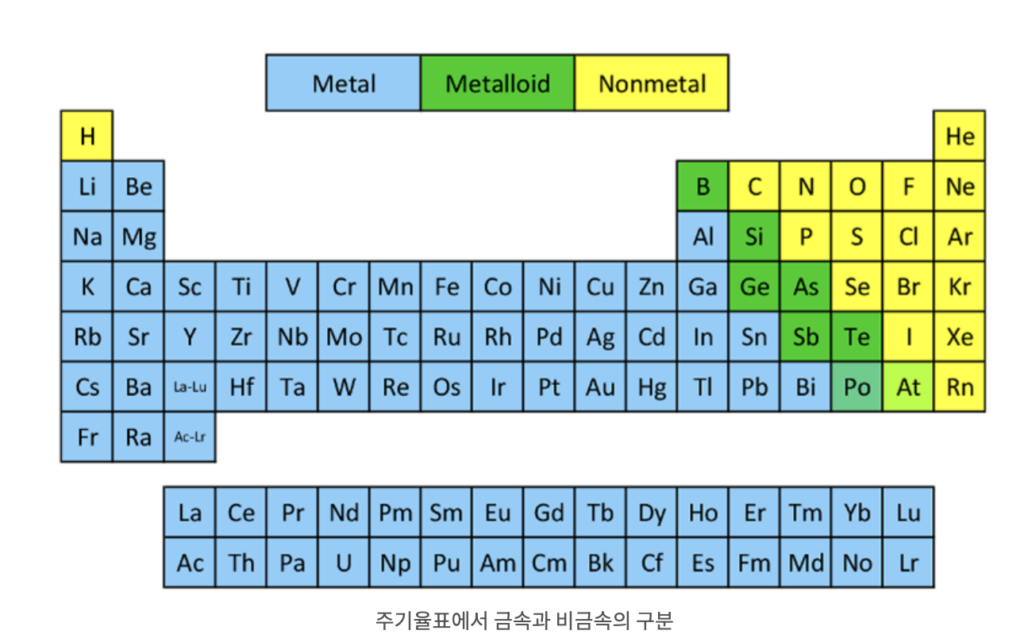
‘왜 갑자기 주기율표죠?😠 라는 분도 계시겠지만
원자의 구분을 통해서 양이온 파와 음이온 파를 확인할 수 있습니다.
간략히 줄여서
금속(metal) = 양(🐑)이온
비금속(nonmetal) = 음(🐮)이온
이 되는 경향이 있습니다.
“준금속은요?”🙋♂️
그렇죠. 준금속도 있습니다.
이녀석들은 비금속과 같이 전자를 받아들이는 걸 좋아해요.
즉, 음이온이 되는 걸 선호하죠.
“어? 불활성기체들은 이온화가 안되는거 아닌가요?”🧐
일반적으로 불황성기체나 Carbon 같은 원소들은
안정된 상태에서 이온화가 되지 않습니다.
하지만 플라즈마와 같은 극한의 상황이 오면
전자를 잃어 버리는 경향이 있죠.
이를 통해 우리는 플라즈마를 유지할 수 있습니다.
이제 장비로 들어가보죠
장비명
IC(ion chromatography, 이온크로마토그래피)
IC 대표 분석물질
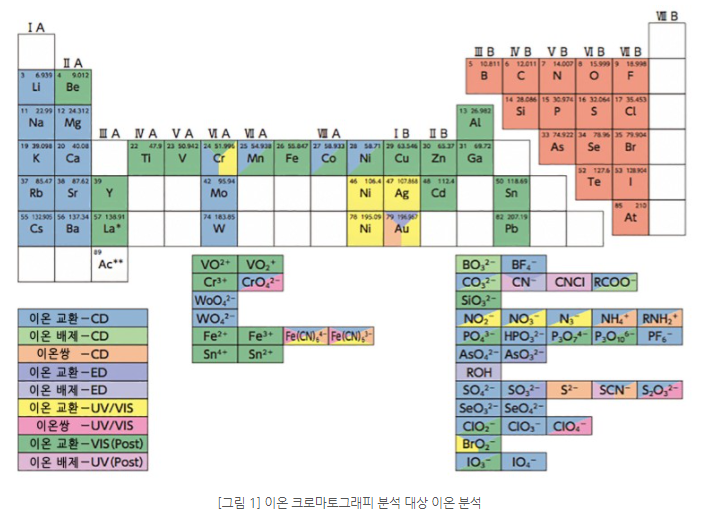
이온화가 가능한 원소 분석이 가능하다.
하지만 각 장비에 이온교환 수지의 종류에 따라 분석이 제한된다.
이를 명확하게 확인하여 어떤 이온인지 어떤 이온 수지가 장착되어 있는 장비를
사용해야 할지 선정할 필요가 있다.
- 애니온 교환 수지 (Anion Exchange Resin): 애니온 교환 수지는 양이온을 교환하기 위해 설계된 수지로, 주로 음이온을 분리하는 데 사용됩니다. 일반적으로 양이온을 가지고 있는 이온교환 수지로, 소듐(Sodium, Na⁺)나 클로라이드(Cl⁻)와 같은 음이온을 교환하여 분리합니다.
- 카티온 교환 수지 (Cation Exchange Resin): 카티온 교환 수지는 음이온을 교환하기 위해 설계된 수지로, 주로 양이온을 분리하는 데 사용됩니다. 일반적으로 음이온을 가지고 있는 이온교환 수지로, 수소(Hydrogen, H⁺)나 암모늄 이온(NH₄⁺)과 같은 양이온을 교환하여 분리합니다.
- 혼성 교환 수지 (Mixed Bed Resin): 혼성 교환 수지는 애니온 및 카티온 교환 수지를 혼합한 것입니다. 이는 양이온과 음이온을 모두 분리하고 정제하는 데 사용됩니다.
- 특정 이온 선택 교환 수지: 특정 이온을 선택적으로 분리하기 위해 특별히 설계된 수지로, 특정 이온에 맞게 선택적으로 작용합니다. 이러한 교환 수지는 특정 이온을 분리하고 정량하는 데 사용됩니다.
기관별 분석가능 원소
| 기관 | 원소 |
| J사 | F–, Cl–, NO2–, Br–, NO3–, PO43-, SO42-,CH3COO−,HCOO−,NH4+ |
분석 할수 있는 것들
- 온성 물질의 분석: 이온화된 화합물을 분리하고 분석하여 화합물의 정량과 동시에 이온성 물질의 특성을 평가합니다.
- 환경, 식품, 의약품 분석: 이온크로마토그래피는 환경 오염물질, 식품 성분, 의약품 등에서 이온성 물질을 분석하는 데 사용됩니다.
- 수질 품질 평가: 이온크로마토그래피는 수질의 이온성 물질을 분석하여 수질의 품질을 평가하는 데 활용됩니다.
이온화가 불가능 한 것들은 분석할 수 없다.
단위검출한계
가장 범용적으로 ppm단위가 사용된다.👍
- ppb~ppm (parts per b/m): 대부분의 경우 IC 결과에서 이온 농도가 ppm 단위로 보고됩니다.
- μg/L (micrograms per liter): 리터 당 마이크로그램으로 표시되는 이온 농도입니다.
- mM (millimolar): 몰 당 1,000분의 1로, 몰농도를 표시하는 데 사용될 수 있습니다.
시편규격
IC는 용액시료만 주입이 가능하다.
| 구분 | 내용 |
| 용액 | 5ml 이상 |
| 고체 | 별도 용액화 전처리 필요 |
장비이론
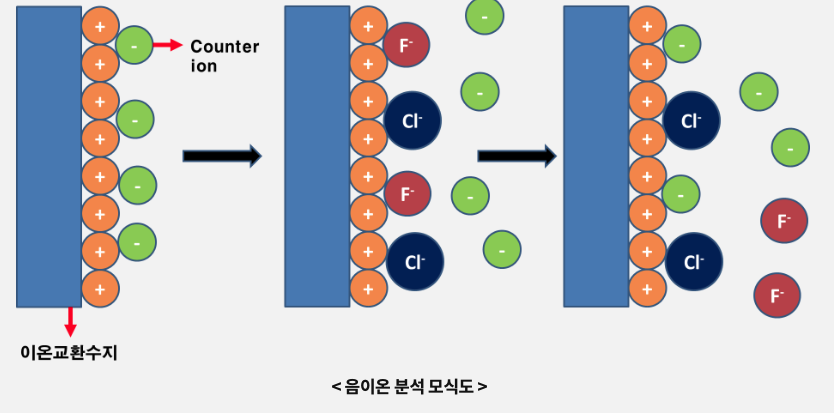
자석의 이론과 비슷하다. 물질들은 이온화가 되면 전기적 특성을 띄게 되는데,
그때 양극자, 음극자를 띄게 된다. 알다 싶이 양극과 음극은 서로 결합하려는 성질로
둘은 끌어당기게 된다. 이로인해 전기적 극성의 정도에 따라서 분리가 일어난다.
위에 그림을 보면 F–, Cl–가 이온컬럼을 지나갈때 +로 인해서 벽에 달라붙는다.
이때 전기적에너지가 약한 F–가 먼저 떨어져서 나가게 된다. 이걸로 어떤 성분인지
확인하는 정량이 가능하다.
분석결과해석
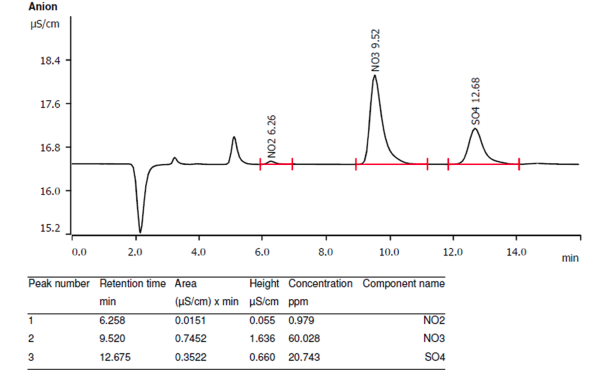
<음이온 분석결과>
x축은 전도도를 나타내는 단위이다. 전기를 얼마나 잘 전달하는지를 보는 것이다.
(x축 지표는 필요에 따라 변경될수 있다.)
y축은 시간이다.
이것으로 해석하면 시간이 지남에 따라 나타나는 전도도를 띈 이온을 본 결과이다.
시간상 가장 빠르게 나온 NO2가 SO4에 비해 전도도가 낮은 것이다.
즉 컬럼에 못달라 붙어서 일찍 나왔다는 이야기가 되겠다.
- 이온화합물은 전하를 가진 이온들로 이루어진 화합물을 의미합니다. 이때, 양전하를 가지는 이온은 양이온(positive ion), 음전하를 가지는 이온은 음이온(negative ion)이라고 합니다. 화합물이 이온으로 이루어져 있으면, 그 전하 상태에 따라 전기적으로 중성이 될 수도 있고 이온 간에 전기적인 상호작용이 일어날 수도 있습니다.
이온화합물은 대부분의 염(예: 염화나트륨 – NaCl), 산 및 염기 (예: 염산 – HCl, 수산화나트륨 – NaOH), 그리고 다양한 종류의 이온성 화합물에 해당합니다. 다양한 이온이 서로 결합하여 안정한 화합물을 형성합니다.
예를 들어, 염화나트륨(NaCl)은 양이온인 나트륨이(Na⁺)와 음이온인 염소이온(Cl⁻)로 이루어진 이온화합물입니다. 나트륨이 양전하를 갖고 있고, 염소는 음전하를 갖고 있기 때문에 이 두 이온은 전기적으로 서로 결합하여 안정한 상태가 됩니다.
이온화합물은 용해성, 전기전도성 등 여러 물리적 및 화학적 특성을 가지고 있어 다양한 분야에서 중요한 역할을 합니다. ↩︎
